جدول تناوبی
۱۵ عنصر فلزی از اکتینیم (با عدد اتمی ۸۹) تا لورنسیم (با عدد اتمی ۱۰۳) واقع در دورهٔ هفتم جدول تناوبی را اکتینیدها میگویند. این نام از نام عنصر اکتینیم گرفته شدهاست. خواص شیمیایی این عناصر شبیه به عنصر اکتینیم است. همهٔ این عنصرها به جز لورنسیم جزو بلوک اف هستند. لورنسیم جزو بلوک دی است اما خواص شیمیاییاش مششابه با چهاردهتای دیگر است. برعکس عنصرهای لانتانید، تنها سه عنصر اول این ردیف (توریم، پروتاکتینیوم و اورانیوم) در طبیعت یافت میشوند. از عنصر چهارم این سری به بعد که عنصرهای ترانس اورانیوم نام دارند، در طبیعت یافت نمیشوند و همگی رادیواکتیو هستند. در این عنصرها ساختارهسته نسبت به آرایش الکترونی از اهمیت کاربردی بیش تری برخورداراست. همه اکتینیدها هسته ناپایداری دارند، به این علت که ازجمله عنصرهای پرتوزا به شمار میآیند. شاید مشهورترین اکتینید، اورانیوم باشد که از فروپاشی هسته آن انرژی لازم برای تولید برق در نیروگاهها، زیر دریاییها و ناوهای هواپیمابر فراهم میشود.
| ۸۹Ac | ۹۰Th | ۹۱Pa | ۹۲U | ۹۳Np | ۹۴Pu | ۹۵Am | ۹۶Cm | ۹۷Bk | ۹۸Cf | ۹۹Es | ۱۰۰Fm | ۱۰۱Md | ۱۰۲No | ۱۰۳Lr |
|
|
خواص
| [نهفتن]Property | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Core charge | ۸۹ | ۹۰ | ۹۱ | ۹۲ | ۹۳ | ۹۴ | ۹۵ | ۹۶ | ۹۷ | ۹۸ | ۹۹ | ۱۰۰ | ۱۰۱ | ۱۰۲ | ۱۰۳ |
| جرم اتمی | [۲۲۷] | ۲۳۲٫۰۳۸۱ | ۲۳۱٫۰۳۵۸۸ | ۲۳۸٫۰۲۸۹۱ | [۲۳۷] | [۲۴۴] | [۲۴۳] | [۲۴۷] | [۲۴۷] | [۲۵۱] | [۲۵۲] | [۲۵۷] | [۲۵۸] | [۲۵۹] | [۲۶۲] |
| تعداد ایزوتوپهای طبیعی | ۳ | ۱ | ۲ | ۳ | ۱ | ۲ | — | — | — | — | — | — | — | — | — |
| Longest-lived isotope | ۲۲۷ | ۲۳۲ | ۲۳۱ | ۲۳۸ | ۲۳۷ | ۲۴۴ | ۲۴۳ | ۲۴۷ | ۲۴۷ | ۲۵۱ | ۲۵۲ | ۲۵۷ | ۲۵۸ | ۲۵۹ | ۲۶۲ |
| نیمهعمر of the longest-lived isotope | ۲۱٫۸ years | ۱۴ billion years | ۳۲٬۵۰۰ years | ۴٫۴۷ billion years | ۲٫۱۴ million years | ۸۰٫۸ million years | ۷٬۳۷۰ years | ۱۵٫۶ million years | ۱٬۴۰۰ years | ۹۰۰ years | ۱٫۲۹ years | ۱۰۰٫۵ days | ۵۲ days | ۵۸ min | ۲۶۱ min |
| Electronic configuration in the ground state | ۶d۱۷s۲ | ۶d۲۷s۲ | ۵f۲۶d۱۷s۲or 5f۱۶d۲۷s۲ | ۵f۳۶d۱۷s۲ | ۵f۴۶d۱۷s۲or 5f۵۷s۲ | ۵f۶۷s۲ | ۵f۷۷s۲ | ۵f۷۶d۱۷s۲ | ۵f۹۷s۲or 5f۸۶d۱۷s۲ | ۵f۱۰۷s۲ | ۵f۱۱۷s۲ | ۵f۱۲۷s۲ | ۵f۱۳۷s۲ | ۵f۱۴۷s۲ | ۵f۱۴۷s۲۷p۱ |
| Oxidation state | ۳ | ۳، ۴ | ۳، ۴، ۵ | ۳، ۴، ۵، ۶ | ۳، ۴، ۵، ۶، ۷ | ۳، ۴، ۵، ۶، ۷ | ۲، ۳، ۴ | ۳، ۴ | ۳، ۴ | ۲، ۳ | ۲، ۳ | ۲، ۳ | ۲، ۳ | ۲، ۳ | ۳ |
| Metallic radius، nm | ۰٫۲۰۳ | ۰٫۱۸۰ | ۰٫۱۶۲ | ۰٫۱۵۳ | ۰٫۱۵۰ | ۰٫۱۶۲ | ۰٫۱۷۳ | ۰٫۱۷۴ | ۰٫۱۷۰ | ۰٫۱۸۶ | ۰٫۱۸۶ | — | — | — | — |
| Ionic radius، nm: An۴+ An۳+ |
— ۰٫۱۲۶ |
۰٫۱۱۴ — |
۰٫۱۰۴ ۰٫۱۱۸ |
۰٫۱۰۳ ۰٫۱۱۸ |
۰٫۱۰۱ ۰٫۱۱۶ |
۰٫۱۰۰ ۰٫۱۱۵ |
۰٫۰۹۹ ۰٫۱۱۴ |
۰٫۰۹۹ ۰٫۱۱۲ |
۰٫۰۹۷ ۰٫۱۱۰ |
۰٫۰۹۶ ۰٫۱۰۹ |
۰٫۰۸۵ ۰٫۰۹۸ |
۰٫۰۸۴ ۰٫۰۹۱ |
۰٫۰۸۴ ۰٫۰۹۰ |
۰٫۰۸۴ ۰٫۰۹۵ |
۰٫۰۸۳ ۰٫۰۸۸ |
| Temperature، °C: melting boiling |
۱۰۵۰ ۳۳۰۰ |
۱۷۵۰ ۴۸۰۰ |
۱۵۷۲ ۴۴۰۰ |
۱۱۳۰ ۳۸۰۰ |
۶۴۰ ۳۹۰۰ |
۶۴۰ ۳۲۳۰ |
۱۱۷۶ ۲۶۱۰ |
۱۳۴۰ — |
۱۰۵۰ — |
۹۰۰ — |
۸۶۰ — |
۱۵۳۰ — |
۸۳۰ — |
۸۳۰ — |
۱۶۳۰ — |
| Density، g/cm۳ | ۱۰٫۰۷ | ۱۱٫۷۸ | ۱۵٫۳۷ | ۱۹٫۰۶ | ۲۰٫۲۵ | ۱۹٫۸۴ | ۱۱٫۷ | ۱۳٫۵۱ | ۱۴٫۷۸ | ||||||
| Standard electrode potential، V: E° (An۴+/An۰) E° (An۳+/An۰) |
— −۲٫۱۳ |
−۱٫۸۳ — |
−۱٫۴۷ — |
−۱٫۳۸ −۱٫۶۶ |
−۱٫۳۰ −۱٫۷۹ |
−۱٫۲۵ −۲٫۰۰ |
−۰٫۹۰ −۲٫۰۷ |
−۰٫۷۵ −۲٫۰۶ |
−۰٫۵۵ −۱٫۹۶ |
−۰٫۵۹ −۱٫۹۷ |
−۰٫۳۶ −۱٫۹۸ |
−۰٫۲۹ −۱٫۹۶ |
— −۱٫۷۴ |
— −۱٫۲۰ |
- −۲٫۱۰ |
| Color [M(H۲O)n]۴+ [M(H۲O)n]۳+ |
— Colorless |
Colorless Blue |
Yellow Dark blue |
Green Purple |
Yellow-green Purple |
Brown Violet |
Red Rose |
Yellow Colorless |
نخودی (رنگ) Yellow-green |
Green Green |
— Pink |
— — |
— — |
— — |
— — |
| Oxidation state | ۸۹ | ۹۰ | ۹۱ | ۹۲ | ۹۳ | ۹۴ | ۹۵ | ۹۶ | ۹۷ | ۹۸ | ۹۹ |
| +۳ | Ac۳+ | Th۳+ | Pa۳+ | U۳+ | Np۳+ | Pu۳+ | Am۳+ | Cm۳+ | Bk۳+ | Cf۳+ | Es۳+ |
| +۴ | Th۴+ | Pa۴+ | U۴+ | Np۴+ | Pu۴+ | Am۴+ | Cm۴+ | Bk۴+ | Cf۴+ | ||
| +۵ | PaO۲+ | UO۲+ | NpO۲+ | PuO۲+ | AmO۲+ | ||||||
| +۶ | UO۲۲+ | NpO۲۲+ | PuO۲۲+ | AmO۲۲+ | |||||||
| +۷ | NpO۲۳+ | PuO۲۳+ | [AmO۶]۵- |
- خواص فیزیکی
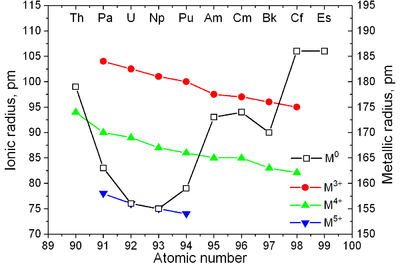 | |
| Major crystal structures of some actinides vs. temperature | Metallic and ionic radii of actinides[۲] |


| [نمایش]لانتانیدها | Ln۳+، Å | Actinides | An۳+، Å | An۴+، Å |
|---|
-

Uranyl nitrate (UO۲(NO۳)۲).
-

Aqueous solutions of uranium III, IV, V, VI salts.
-

Aqueous solutions of neptunium III, IV, V, VI, VII salts.
-

Aqueous solutions of plutonium III, V, VI, VII salts.
-

تتراکلرید اورانیوم.
-

هگزافلوراید اورانیوم.
-

U۳O۸ (yellowcake).
ترکیبها
- اکسیدها و هیدروکسیدها
| [نمایش]ترکیب | رنگ | ساختار شیمیایی، نوع | ثابت شبکه بلوری، Å | چگال، g/cm۳ | دما، °C | ||
|---|---|---|---|---|---|---|---|
| [نمایش]Oxidation state | ۸۹ | ۹۰ | ۹۱ | ۹۲ | ۹۳ | ۹۴ | ۹۵ | ۹۶ | ۹۷ | ۹۸ | ۹۹ |
|---|
| فرمول شیمیایی | ThO۲ | PaO۲ | UO۲ | NpO۲ | PuO۲ | AmO۲ | CmO۲ | BkO۲ | CfO۲ |
| شماره ثبت سیایاس | ۱۳۱۴-۲۰-۱ | ۱۲۰۳۶-۰۳-۲ | ۱۳۴۴-۵۷-۶ | ۱۲۰۳۵-۷۹-۹ | ۱۲۰۵۹-۹۵-۹ | ۱۲۰۰۵-۶۷-۳ | ۱۲۰۱۶-۶۷-۰ | ۱۲۰۱۰-۸۴-۳ | ۱۲۰۱۵-۱۰-۰ |
| PubChem | ۱۴۸۰۸ | ۱۰۹۱۶ | |||||||
| جرم مولی | ۲۶۴٫۰۴ | ۲۶۳٫۰۳۵ | ۲۷۰٫۰۳ | ۲۶۹٫۰۴۷ | ۲۷۶٫۰۶۳ | ۲۷۵٫۰۶ | ۲۷۰–۲۸۴** | ۲۷۹٫۰۶۹ | ۲۸۳٫۰۷۸ |
| نقطه ذوب | ۳۳۹۰ °C | ۲۸۷۸ °C | ۲۶۰۰ °C | ۲۴۰۰ °C | ۲۰۵۰ °C | ||||
| نقطه جوش | ۴۴۰۰ °C | ۲۸۰۰ °C | |||||||
| ساختار |  An۴+: __ / O۲−: __ | ||||||||
| گروه فضایی | Fm۳m | ||||||||
| عدد کوئوردیناسیون | An[۸], O[۴] | ||||||||
- An – اکتینید
**بسته به ایزوتوپها
- نمکها
| فرمول شیمیایی | AcCl۳ | UCl۳ | NpCl۳ | PuCl۳ | AmCl۳ | CmCl۳ | BkCl۳ | CfCl۳ |
| شماره ثبت سیایاس | ۲۲۹۸۶-۵۴-۵ | ۱۰۰۲۵-۹۳-۱ | ۲۰۷۳۷-۰۶-۸ | ۱۳۵۶۹-۶۲-۵ | ۱۳۴۶۴-۴۶-۵ | ۱۳۵۳۷-۲۰-۷ | ۱۳۵۳۶-۴۶-۴ | ۱۳۵۳۶-۹۰-۸ |
| PubChem | ۱۶۷۴۴۴ | |||||||
| جرم مولی | ۳۳۳٫۳۸۶ | ۳۴۴٫۳۸۷ | ۳۴۳٫۴۰۶ | ۳۵۰٫۳۲ | ۳۴۹٫۴۲ | ۳۴۴–۳۵۸** | ۳۵۳٫۴۲۸ | ۳۵۷٫۴۳۸ |
| نقطه ذوب | ۸۳۷ °C | ۸۰۰ °C | ۷۶۷ °C | ۷۱۵ °C | ۶۹۵ °C | ۶۰۳ °C | ۵۴۵ °C | |
| نقطه جوش | ۱۶۵۷ °C | ۱۷۶۷ °C | ۸۵۰ °C | |||||
| ساختار بلوری| Colspan = "8"|
An۳+: __ / Cl−: __ | ||||||||
| گروه فضایی | P۶۳/m | |||||||
| عدد کوئوردیناسیون | An*[۹], Cl [۳] | |||||||
| ثابت شبکه بلوری | a = ۷۶۲ pm c = ۴۵۵ pm |
a = ۷۴۵٫۲ pm c = ۴۳۲٫۸ pm |
a = ۷۳۹٫۴ pm c = ۴۲۴٫۳ pm |
a = ۷۳۸٫۲ pm c = ۴۲۱٫۴ pm |
a = ۷۲۶ pm c = ۴۱۴ pm |
a = ۷۳۸٫۲ pm c = ۴۱۲٫۷ pm |
a = ۷۳۸ pm c = ۴۰۹ pm | |
*An – اکتینید
فلز واسطه
عناصر واسطه، همگی خصلت فلزی دارند. از نظر موقعیت در جدول تناوبی از دوره چهارم به بعد دو عنصر اصلی اول و شش عنصر اصلی آخر دوره در ده خانه، قرار دارند. از نظر آرایش الکترونی بر عکس فلزات قلیایی و قلیایی خاکی همدوره خود، سطح انرژی تراز n-۱)d) لایه ظرفیت آنها از سطح تراز ns این لایه پایینتر است. از اینرو آخرین الکترون اتم آنها در n-۱)d) وارد میشود و تراز p لایه ظرفیت و اتم آنها از الکترون خالیست.
طبقه بندی عناصر واسطه
این عنصرها بسته به اینکه الکترون متمایز کننده اتم آنها در تراز n-۱)d) و یا در تراز n-۲)f) لایه ظرفیت وارد شود، به دو دسته تقسیم میشوند.
| گروه | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
|---|---|---|---|---|---|---|---|---|---|---|
| تناوب 4 | Sc 21 | Ti 22 | V 23 | Cr 24 | Mn 25 | Fe 26 | Co 27 | Ni 28 | Cu 29 | Zn 30 |
| تناوب 5 | Y 39 | Zr 40 | Nb 41 | Mo 42 | Tc 43 | Ru 44 | Rh 45 | Pd 46 | Ag 47 | Cd 48 |
| تناوب 6 | * 57–71 | Hf 72 | Ta 73 | W 74 | Re 75 | Os 76 | Ir 77 | Pt 78 | Au 79 | Hg 80 |
| تناوب 7 | ** 89–103 | Rf 104 | Db 105 | Sg 106 | Bh 107 | Hs 108 | Mt 109 | Ds 110 | Rg 111 | Cn 112 |
| گروه | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
|---|---|---|---|---|---|---|---|---|---|---|
| تناوب 4 | Sc 21 | Ti 22 | V 23 | Cr 24 | Mn 25 | Fe 26 | Co 27 | Ni 28 | Cu 29 | Zn 30 |
| تناوب 5 | Y 39 | Zr 40 | Nb 41 | Mo 42 | Tc 43 | Ru 44 | Rh 45 | Pd 46 | Ag 47 | Cd 48 |
| تناوب 6 | * 57–71 | Hf 72 | Ta 73 | W 74 | Re 75 | Os 76 | Ir 77 | Pt 78 | Au 79 | Hg 80 |
| تناوب 7 | ** 89–103 | Rf 104 | Db 105 | Sg 106 | Bh 107 | Hs 108 | Mt 109 | Ds 110 | Rg 111 | Cn 112 |
فلزات واسطه دسته d
الکترونهای متمایز کننده اتم این عنصرها در تراز n-۱)d) لایه ظرفیت اتم آنها وارد میشود و عموما (غیر از روی و کادمیم)، در حالت اکسایش صفر و یا دست کم در یکی از حالتهای اکسایش بالاتر از صفر، یک یا چند اوربیتال تک الکترونی در تراز لایه ظرفیت اتم خود دارند. عنصرهای واسطه دوره چهارم (ردیف ۳d)، دوره پنجم (ردیف ۴d)، دوره ششم (ردیف ۵d) و دوره هفتم (ردیف ۶d)، جزو این دسته از فلزات هستند.
فلزات واسطه دسته F
این عناصر که الکترونهای متمایز کننده اتم آنها، در ترازهای n-۲)F) لایه ظرفیت که ترازهای نسبتا درونیاند قرار میگیرند، به عناصر واسطه داخلی معروفند و جزو عنصرهای گروه III B در جدول تناوبی میباشند و دو ردیف متمایز از عنصرهای واسطه را شامل میشوند که عبارتند از اکتنیدها و لانتانیدها.
خواص فیزیکی عناصر واسطه
به غیر از عناصر واسطه گروه II B (یعنی روی، کادمیم، جیوه) و فلزهای واسطه دیگر)، دماهای ذوب و جوش، گرمای نهان تبخیر، چگالی، سختی، انرژی بستگی نسبتا بالایی دارند (در بین آنها تنها جیوه در دمای معمولی مایع است). شدت این خواص در عنصرهای واسطه میانی هر ردیف بیشتر میشود. دلیل این رویداد، وجود اوربیتالهای تک الکترونی نسبتا زیاد در تراز d و امکان همپوشانی مناسب این اوربیتالها، تشکیل پیوند کووالانسی در شبکه بلور و افزایش انرژی بستگی بلور فلزی است. اما در آخرین عنصر واسطه هر ردیف، انرژی بستگی به پایینترین حد خود نزول میکند.
خواص مکانیکی عناصر واسطه
فلزهای واسطه عموما انعطاف پذیرند، قابلیت تغییر شکل دارند، خاصیت چکش خواری، صیقل پذیری، تورّق و مفتول شدن آنها خیلی زیاد است. در مقابل ضربه، فشار و کشش، مقاومت دارند (غیر از جیوه که مایع، روی و کروم که شکنندهاند).
البته فلزهای گروه IB (مس، نقره و طلا) بسیار نرماند. این فلزها با یکدیگر و نیز با برخی نافلزات، آلیازهای بسیار مهمی تشکیل میدهند که خواص و کاربردهای ویژهای در پژوهش، علم و صنعت دارند. از آلیاژ این فلزات در ساخت موتور جت هواپیما، استفاده میشود.

خواص مغناطیسی
این فلزها عموما (غیر از روی و کادمیم) در حالت آزاد و خنثی و یا دست کم در یکی از حالتهای اکسایش خود در ترکیبها، دارای اوربیتالهای تک الکترونیاند. از اینرو، غالبا در حالت گازی یا در بسیاری از ترکیبات کوئوردیناسیون خود، بویژه با لیگاندهای ضعیف دارای خاصیت پارامغناطیسیاند. بدیهی است برخی از آنها که فاقد الکترون جفتنشدهاند، حتی در حالت آزاد (گازی) دارای خاصیت دیامغناطیسیاند (مانند روی و کادمیم) و یا ممکن است برخی از آنها با داشتن الکترونهای جفتنشده در بلور، آنتی فرومغناطیس باشند و یا در ترکیبات کمپلکس یا لیگاندهای قوی و یا مغناطیس باشند (کروم).الکترونگاتیوی
به علت کوچک بودن اندازه اتم و زیاد بودن بار موثر هسته، عنصرهای واسطه نسبت به عنصرهای اصلی، الکترونگاتیوی و انرژی یونش عنصرهای واسطه نسبت به عنصرهای اصلی همدوره خود بیشتر است.رسانایی برق و گرما
فلزات واسطه، عموما جریان برق را به خوبی هدایت میکنند، قدرت رسانایی عنصرهای گروه IB از فلزهای دیگر بیشتر است، (دلیل آن پر بودن اوربیتالهای تراز d و وجود اوربیتال تک الکترونی S لایه ظرفیت است). رسانایی گرمایی این فلزات به موازات رسانایی الکتریکی آنها افزایش مییابد. رسانایی الکتریکی وانادیوم از فلزهای دیگر کمتر است.فلزات واسطه خارجی
این دسته از فلزات را میتوان در خود جدول تناوبی مشاهده نمود، در عناصر واسطه خارجی زیر لایهٔ d در حال پرشدن میباشد، این عناصر نسبت به فلزات گروه اول و دوم سختی، چگالی و دمای ذوب و جوش بالاتری دارند، همه فلزات (اعم از قلیایی، قلیایی خاکی و واسطه و فلزات اصی دسته p) جامد میباشند به جز جیوه که در دمای اتاق به حالت مایع میباشد و یک استثناء به شمار میآید. در آرایش الکترونی این عناصر بی نظمیهای متعددی دیده میشود، برای مثال دو نمونه از این بی نظمیها در دو عنصر Cr و Cu دیده میشوند، گروه یازدهم یا IB با نام فلزات سکه ساز نیز شناخته میشوند که شامل سه عنصر مس، نقره و طلا میباشد، البته در بین فلزات واسطه خارجی نامگذاریهای دیگری نیز وجود دارد که به صورت دستهای صورت گرفتهاند و نظمی بین این دسته بندیها دیده نمیشود، برای مثال دو نمونه از این دسته بندیها عبارتند از:
- فلزات پلاتینی: که شامل شش عنصر پالادیم، پلاتین، رودیم، ایریدیم، روتنیم و اوسمیم میباشد.
- تریادها یا فلزات فرومانتیک یا دستهٔ سه تاییها: که شامل آهن، کبالت و نیکل سه عنصر که در نامگذاری آیوپاک در یک گروه قرار گرفتهاند و در تناوب چهارم جدول تناوبی و گروههای هشتم و نهم و دهم قراردارند.
فلزات واسطه داخلی
با مشاهدهٔ جدول تناوبی دو دسته از عناصر را مشاهده میکنید که جدا از جدول تناوبی و در پایین تصویر قرار گرفتهاند، اینها همان عناصر واسطهٔ داخلی هستند که عناصر دستهٔ اول خواصی مشابه فلز لانتان دارند و به لانتانیدها مشهور هستند و عناصر دستهٔ دوم خواصی مشابه فلز اکتینیم دارند و به اکتینیدها معروف شدهاند.
از آن جا که قرار دادن لانتانیدها و اکتینیدها در خانههای پلاک ۵۷ و ۸۹ میسرنمی شد، این دو گروه در پایین جدول تناوبی و به صورت جداگانه اما با ارجاع به دو عنصر لانتانیم(لانتان) و اکتینیم قرارگرفتهاند.
لانتانیدها: در این عناصر زیرلایهٔ ۴f در حال پرشدن میباشد و شامل عناصر از عدد اتمی ۵۸ تا ۷۱ میباشند.
اکتینیدها: در این عناصر زیرلایهٔ ۵f در حال پرشدن میباشد و شامل عناصر از عدد اتمی ۹۰ تا ۱۰۳ میباشد، برای مطالعهٔ اکتینیدها ساختارهسته نسبت به آرایش الکترونی عناصر از اهمیت بیش تری برخوردار میباشد، مشهورترین اکتینید که امروزه بحثهای زیادی را در اقتصاد و سیاست و علم به خود اختصاص دادهاست اورانیوم میباشد که از آن انواع استفادههای صلح آمیز و غیر صلح آمیز(برای ساخت سلاحهای شیمیایی) میشود.
از ترکیب فلزات واسطه خارجی با ترکیبات آلی ترکیبات آلی فلزی مهمی با کاربردهای گوناگون تشکیل میشوند.
شبهفلزات
شبهفلز، یک عنوان برای طبقهبندی عناصر شیمایی است. که به عناصری اطلاق میگردد که خواصشان میان فلز و نافلز است.
تعریف معینی برای شبه فلزها وجود ندارد اما دو خاصیت زیر مشخصه آنها است:
- شبهفلزها معمولاً به شکل اکسیدهای آمفوتر یافت میشوند.
- شبهفلزها معمولاً نیمهرسانا هستند
| ۱۳ | ۱۴ | ۱۵ | ۱۶ | ۱۷ | |
|---|---|---|---|---|---|
| ۲ | B بور |
C کربن |
N نیتروژن |
O اکسیژن |
F فلوئور |
| ۳ | Al آلومینیوم |
Si سیلیسیوم |
P فسفر |
S گوگرد |
Cl کلر |
| ۴ | Ga گالیوم |
Ge ژرمانیوم |
As آرسنیک |
Se سلنیوم |
Br برم |
| ۵ | In ایندیوم |
Sn قلع |
Sb آنتیموان |
Te تلوریوم |
I ید |
| ۶ | Tl تالیوم |
Pb سرب |
Bi بیسموت |
Po پولونیوم |
At استاتی |
نافلزها
نافلز، گروهی در عناصر شیمیایی است.در جدول تناوبی عناصر یا فلز هستند یا نافلز و یا شبه فلز
نا فلزات عبارتند از:
- هیدروژن (H)
- در گروه ۱۴: کربن (C)
- در گروه ۱۵: نیتروژن (N)، فسفر (P)
- در گروه ۱۶: اکسیژن (O)، گوگرد (S)، سلنیوم (Se)
- گروه ۱۷ - هالوژنها
- تمام اعضای گروه ۱۸(گازهای نجیب)
هالوژن
گروه هالوژن عناصر گروه ۱۷ (گروه ۷ اصلی) جدول تناوبی هستند یعنی: فلوئورF، کلرCl، برمBr، یدI و استاتینAt.
هالوژنها (به انگلیسی: Halogen) در حالت طبیعی خود مولکولهای دواتمی هستند.
واژهٔ هالوژن از زبان یونانی گرفته شده و به معنی نمکزا است.
| هالوژن | جرم اتمی | نقطه ذوب | نقطه جوش | الکترونگاتیویته |
|---|---|---|---|---|
| فلوئور | ۱۹ | ۵۳/۵۳ | ۸۵/۰۳ | ۳/۹۸ |
| کلر | ۳۵/۵ | ۱۷۱/۶ | ۲۳۹/۱۱ | ۳/۱۶ |
| برم | ۸۰ | ۲۶۵/۸ | ۳۳۲/۰ | ۲/۹۶ |
| ید | ۱۲۷ | ۳۹۶/۸۵ | ۴۵۷/۴ | ۲/۶۶ |
| استاتین | ۲۱۰ | ۵۷۵ | ۶۱۰ | ۲/۲ |
گاز نجیب
گازهای نجیب[۱] (یا گازهای کمیاب یا گازهای بیاثر) که بی بو، و بی رنگ هستند، به عنصرهای هلیوم، نئون، آرگون، کریپتون، گزنون، رادون و آناناکتیوم گفته میشود که همه در دمای اتاق گازی هستند.
گازهای نجیب بی رنگ و بی بو بوده و در گروه A8 جدول مندلیف قرار دارند. این گروه گازها شامل هلیم ، نیون ، آرگون ، کریپتون ، زنون و رادون است. به استثنای هلیم ، تمام گازهای نجیب دارای آرایش الکترونی خارجی ns2 np6 هستند که آرایشهای بسیار پایدارند.
تمامی این گازها تک اتمی بوده و به مقادیر کم در اتمسفر یافت می شود (تنها حدود یک درصد حجم هوا
را تشکیل می دهند). در بین گازهای بی اثر، رادون رادیواکتیو خطرناک می باشد. گازهای بی اثر بیشترین
انرژی یونیزاسیون را داشته و الکترونگاتیویته آنها بسیار کم و ناچیز می باشد. این گازها نقطه ذوب
پایینی داشته (هلیم کمترین مقدار نقطه ذوب را دارد) و همگی در هوای اتاق به شکل گاز می باشند.
تا سال 1960، تصور می شد که این گازها به علت داشتن عدد اکسیداسیون صفر بی اثر بوده و تمایل به تشکیل ترکیب ندارند. تمامی گازهای نجیب ماکزیمم تعداد الکترون را در لایه بیرونی(آخر) الکترونی خود دارا بوده ( گاز هلیم 2 و بقیه گازها 8 الکترون) و تمایلی خیلی اندکی به گرفتن یا از دست دادن الکترون دارند که همین خاصیت موجب پایداری آنها شده است. در مورد گازهای هلیم، نئون و آرگون ترکیبی شناخته شده ای ثبت نشده ولی کریپتون در واکنش با فلوئورین تشکیل جامد بی رنگ می دهد. زنون هم تشکیل ترکیبات زیادی با اکسیژن و فلوئورین می دهد.
ﺧﻮﺍﺹ ﻭ ﺗﺮﻛﻴﺒﻬﺎ
ﺗﺎ ﺳﺎﻝ 1962 ﺗﺼﻮﺭ ﻣﻲﺭﻓﺖ ﻛﻪ ﺍﻳﻦ ﮔﺎﺯﻫﺎ ﺩﺭ ﻭﺍﻗﻊ ﺍﺯ ﻧﻈﺮ ﻓﻌﺎﻟﻴﺖ ﺷﻴﻤﻴﺎﻳﻲ ﺑـﻲﺍﺛﺮﻧـﺪ ﻭﻟـﻲ ﺩﺭ ﺁﻥ ﺳﺎﻝ ﺑﺎﺭﺗﻠﺖ، ﺑﺎ ﺗﻬﻴﻪ ﺗﺮﻛﻴﺒﻲ ﺑﻪ ﻓﺮﻣﻮﻝ O2PtF6 (ﺑﻠﻮﺭﻫﺎﻱ ﻗﺮﻣﺰ ﻧﺎﺭﻧﺠﻲ) ﻭ ﺑﺎ ﺗﻮﺟﻪ ﺑﻪ ﺍﻳﻨﻜﻪ ﺍﻧﺮﮊﻱ ﻳﻮﻧﺶ Xe , O2 ﺑﻬﻢ ﻧﺰﺩﻳﻚ ﺍﺳﺖ (ﺣﺪﻭﺩ 279 ﻛﻴﻠﻮﻛﺎﻟﺮﻱ ﺑﺮ ﻣﻮﻝ) ﺑﻪ ﻓﻜﺮ ﺗﻬﻴﻪ O2PtF6 ﺍﻓﺘﺎﺩ ﻭ ﺳﺮﺍﻧﺠﺎﻡ ﺁﻥ ﺭﺍ ﺑﻪ ﺻﻮﺭﺕ ﺑﻠﻮﺭﻫﺎﻱ ﺯﺭﺩ ﺭﻧﮓ ﺑﺪﺳﺖ ﺁﻭﺭﺩ. ﺑﻪ ﺗﺪﺭﻳﺞ ﺗﺮﻛﻴﺒﻬﺎﻱ ﺩﻳﮕﺮﻱ ﺍﺯ Xe ﺑﺪﺳﺖ ﺁﻣﺪ ﻛﻪ ﺑﻴﺸﺘﺮ ﺁﻧﻬﺎ ﺭﺍ می توان از XeF6 (ﻛﻪ ﺧﻮﺩ ﻣﺎﻧﻨﺪ ﺳﺎﻳﺮ ﻓﻠﻮﺋﻮﺭﻳﺪﻫﺎﻱ ﺯﻧﻮﻥ ﺍﺯ ﺗﺮﻛﻴﺐ ﻣﺴﺘﻘﻴﻢ ﺩﺭ ﺩﻣﺎﻱ ﻗـﻮﺱ ﺍﻟﻜﺘﺮﻳﻜـﻲﺣﺎﺻﻞ ﻣﻲﺷﻮﻧﺪ) ﺑﺪﺳﺖ ﺁﻭﺭﺩ. ﻓﺮﻣﻮﻝ ﻭ ﺳﺎﺧﺘﺎﺭ ﺑﺮﺧﻲ ﺍﺯ ﺍﻳﻦ ﺗﺮﻛﻴﺒﻬﺎ ﺩﺭ ﺟﺪﻭﻝ ﺯﻳﺮ ﻧﺸﺎﻥ ﺩﺍﺩﻩ ﺷﺪﻩ ﺍﺳﺖ.
منبع اصلی گازهای نجیب اتمسفری
تئوری های فعلی پیشنهاد می کنند گاز آرگون موجود در اطراف زمین از ماگماهای آتش فشانی تولید شده است، اما دانشمندان موسسه ی پلی تکنیک رنسلیر نیویورک که نتایج بررسی های خود را در مجله ی نیچر منتشر کرده اند، تحقیقات جدیدی را در این خصوص انجام داده اند.محققان فرضیه ای را مطرح کردند مبنی بر این که این گاز می تواند از پوسته ی اقیانوسی آزاد شده باشد. در حقیقت پوسته ی اقیانوسی برعکس پوسته ی زمینی از کانی هایی ساخته شده است که غنی از آرگون هستند.
ﺭﻭﺵ ﺗﻬﻴﻪ
ﺁﺭﮔﻮﻥ، ﻧﺌﻮﻥ، ﻛﺮﻳﭙﺘﻮﻥ ﻭ ﺯﻧﻮﻥ ﺍﻭﻟﻴﻦ ﺑﺎﺭ ﺑﻴﻦ ﺳـﺎﻟﻬﺎﻱ 1894 ﺗـﺎ 1898 ﺗﻮﺳـﻂ ﺭﺍﻣـﺴﻲ، ﺭﺍﻳﻠـﻪ ﻭ ﺗﺮﺍﻭﺭﺱ ﺍﺯ ﺭﺍﻩ ﺗﻘﻄﻴﺮ ﺟﺰﺀ ﺑﻪ ﺟﺰﺀ ﻫﻮﺍﻱ ﻣﺎﻳﻊ ﺑﺪﺳﺖ ﺁﻣﺪﻧﺪ. ﺭﺍﺩﻭﻥ ﺍﺯ ﺭﺍﻩ ﻭﺍﻛﻨﺸﻬﺎﻱ ﻭﺍﭘﺎﺷﻲ ﺭﺍﺩﻳﻮﺍﻛﺘﻴـﻮﻱ ﺗﻮﺭﻳﻢ ﻭ ﺭﺍﺩﻳﻢ ﺗﻮﺳﻂ ﺩﻭﺭﻥ ﺩﺭ 1900 ﻛﺸﻒ ﺷﺪ.
ﻛﺎﺭﺑﺮﺩﻫﺎﻱ ﻣﻬﻢ
• ﺩﺭ ﺗﻬﻴﻪ ﺗﺎﺑﻠﻮﻫﺎﻱ ﻧﺌﻮﻥ (ﻫﻠﻴﻢ: ﺯﺭﺩ، ﻧﺌﻮﻥ: ﻗﺮﻣﺰ، ﺁﺭﮔﻮﻥ: ﻗﺮﻣﺰ ﻳﺎ ﺁﺑﻲ، ﻛﺮﻳﭙﺘﻮﻥ: ﺳﺒﺰ ﻣﺎﻳﻞ ﺑﻪ ﺁﺑﻲ ﻭ ﺯﻧﻮﻥ: ﺁﺑﻲ ﻣﺘﻤﺎﻳﻞ ﺑﻪ ﺳﺒﺰ). • ﺗﻬﻴﻪ ﻫﻮﺍﻱ ﺗﻨﻔﺴﻲ ﺑﺮﺍﻱ ﻏﻮﺍﺻﻲ، ﺭﻗﻴﻖ ﻛﺮﺩﻥ ﺍﻛﺴﻴﮋﻥ ﺑﺮﺍﻱ ﺗﻨﻔﺲ ﺑﻴﻤﺎﺭﺍﻥ ﻣﺒﺘﻼ ﺑﻪ ﺁﺳـﻢ ﻭ ﺟﻮﺷﻜﺎﺭﻱ. • ﺗﻬﻴﻪ ﻻﻣﭙﻬﺎﻱ ﻓﻠﻮﺭﺳﺎﻥ ﻭ ﻻﻣﭙﻬﺎﻱ ﻣﻌﻤﻮﻟﻲ ﻭ ...


















 وبلاگ مهندسی شیمی با مدیریت یونس کرمی دانشجوی مهندسی شیمی دانشگاه آزاد اسلامی واحد امیدیه .
وبلاگ مهندسی شیمی با مدیریت یونس کرمی دانشجوی مهندسی شیمی دانشگاه آزاد اسلامی واحد امیدیه .